Thủy ngân phát tán ra môi trường, sau vụ cháy nhà kho của Công ty bình minh ở Hà Nội hôm 28/8 là một điều không thể chối cãi. nên chi việc xử lý hậu quả và tiêu độc là một điều tấm của các bên hệ trọng. Nhưng làm thế nào để giảm thiểu và loại bỏ hoàn toàn chúng trong đất, nước và không khí là một vấn đề khôn xiết phức tạp. Vì thế trong bài viết lần này, blog sẽ giúp bạn có cái nhìn rõ nét hơn về các phương pháp tiêu độc thủy ngân.
Trước khi đi vào nội dung chính của bài, chúng ta sẽ tìm hiểu một tẹo về thủy ngân trước nha!
Hóa học của thủy ngân
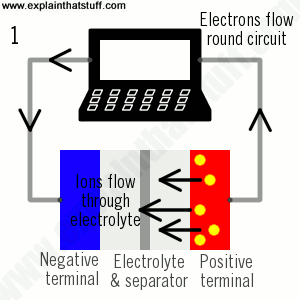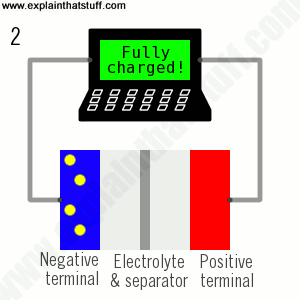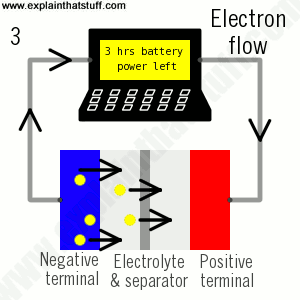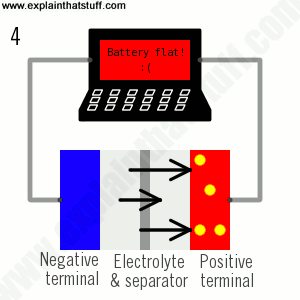
Thủy ngân nhân tố là một chất lỏng màu trắng bạc, nặng ở nhiệt độ phòng. vày sức căng bề mặt cao nên thủy ngân thường tạo thành những giọt hình cầu nhỏ gọn khi được phóng thích trong môi trường. mặc dầu bản thân các giọt ổn định, nhưng áp suất hơi cao của thủy ngân so với các kim khí khác làm cho nó dễ bốc hơi. Do đó, thủy ngân được giải phóng và việc không được phát hiện kịp thời có thể chóng vánh trở thành mối hiểm nguy khi hít phải.
Các trạng thái oxy hóa phổ quát nhất đối với thủy ngân là Hg+1 (mercurous) hoặc Hg+2 (mercuric). Các tính chất và hành vi hóa học của thủy ngân phụ thuộc mạnh mẽ vào trạng thái oxy hóa của nó. Thủy ngân có thể tạo thành một loạt các muối vô cơ và không giống như các kim loại kiềm và kiềm thổ, nó có thể hình thành kết liên cộng hóa trị với các gốc hữu cơ. hồ hết thủy ngân khi ngặp trong nước, đất, trầm tích, quần xã sinh vật và các môi trường khác (trừ khí quyển) tồn tại ở dạng muối thủy ngân vô sinh và hợp chất cơ kim thủy ngân (organomercurics). Các organomercurics được xác định bởi sự hiện diện của liên kết cộng hóa trị C-Hg.
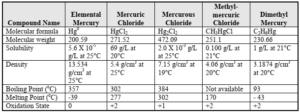
Các hợp chất thủy ngân sau đây thường được tìm thấy trong các điều kiện môi trường như muối thủy ngân HgS, HgCl, Hg (OH) và HgS; ion methylmercury (HgCH3 +) và các hợp chất methylmercuric clorua (CH3HgCl) và hydroxit methylmercuric (CH3HgOH); và một số nhỏ các hợp chất khác của organomercurics (ví dụ, dimethylmercury và phenylmercury). Trong đó, methylmercury có thể gây thương tổn hệ thần kinh, đặc biệt là ở thai nhi và trẻ sơ sinh – hình thành khi thủy ngân xâm nhập vào đất hoặc trầm tích và được tác động bởi các vi sinh vật kỵ khí. Độ hòa tan của các hợp chất thủy ngân khác nhau, từ không đáng kể (HgCl, HgS) đến rất hòa tan (HgCl2). Bạn có thể tham khảo thêm bảng bên dưới nhé!
Các dạng ion của thủy ngân bị hấp phụ mạnh bởi đất và trầm tích và bị khử từ từ. Các khoáng vật đất sét hấp phụ tối ưu các ion thủy ngân ở pH 6. Các oxit sắt cũng hấp phụ các ion thủy ngân trong đất trung tính. Hầu hết các ion thủy ngân được hấp phụ bởi các chất hữu cơ (cốt là axit fulvic và humic) trong đất chua. Khi nào không có chất hữu cơ, thủy ngân trở nên tương đối linh hoạt hơn trong đất axit và có thể bay hơi vào bầu không khí hoặc rỉ nước vào nước ngầm.
Các phương pháp tiêu độc thủy ngân
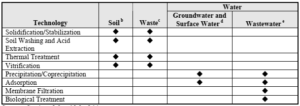
Theo Cơ quan Bảo vệ Môi trường Mỹ (gọi tắt là EPA) thì có 8 phương pháp đã được xác định để xử lý toàn bộ đất, chất thải và nước bị ô nhiễm thủy ngân và được chia ra thành 2 nhóm xử lý chính đó là:
Xử lý đất và chất thải
- Solidification/Stabilization (Hóa rắn / Ổn định)
- Soil Washing (Rửa đất)
- Thermal Treatment (Xử lý nhiệt)
- Vitrification (Thủy tinh hóa)
Xử lý nước
- Precipitation/Coprecipitation (Kết tủa / đồng hóa)
- Adsorption (Hấp phụ)
- Membrane Filtration (Lọc màng)
- Bioremediation (Xử lý sinh học)
Trong đó, kỹ thuật hóa rắn / ổn định được dùng để xử lý thủy ngân yếu tố; các phương pháp còn lại được sử dụng để xử lý các hợp chất thủy ngân.
1. Hóa rắn / Ổn định (gói tắt là S/S)
Mô tả: S/S làm giảm tính di động của các chất độc hại và các chất gây ô nhiễm trong môi trường chuẩn y cả công cụ vật lý và hóa học. Nó kết liên vật lý hoặc bao vây các chất gây ô nhiễm trong một khối ổn định và hóa học làm giảm tiềm năng nguy cơ của chất thải, bằng cách chuyển đổi các chất gây ô nhiễm thành các dạng ít hòa tan, di động hoặc ít độc hại. Sự pha trộn thường được dùng để nhất thiết thủy ngân nhân tố bằng cách hòa tan thủy ngân trong một kim khí khác để tạo thành hợp kim semisolid được gọi là hỗn hống. Quá trình này là bất động vật lý và thường được phối hợp với đóng gói để ngăn ngừa sự bay hơi của thủy ngân từ hỗn hống.
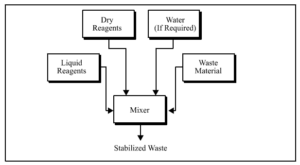
vận dụng:
- Đất
- Bùn
- Chất rắn khác
- Chất thải lỏng
- Chất thải công nghiệp
- Thủy ngân nguyên tố (lỏng)
Chất kết dính và thuốc thử được sử dụng trong S/S:
- Xi măng
- Polysulfide canxi
- Gốm sứ phốt phát liên kết hóa học (CBPC)
- Phốt phát
- Bạch kim
- Nhựa polyester
- Hạt polymer
- Các hợp chất Polysiloxane (silicon hydride và silicon hydroxide)
- Chất điều chỉnh pH
- Natri dithiocarbamate
- Metasilicate natri
- Natri sunfua
- Xi măng polymer sulfur (SPC)
Chất kết dính và thuốc thử được sử dụng trong hỗn hống thủy ngân:
- Đồng
- Thiếc (kẽm)
- Niken
- Kẽm
2. Rửa đất và ly trích acid
biểu thị: Rửa đất là một công nghệ ngoại vi tận dụng lợi thế của hành vi một số chất gây ô nhiễm, để tiếp nhận tốt hơn vào phần bị nhiễm. Đất bị ô nhiễm lơ lửng trong dung dịch rửa và các hạt mịn được tách ra khỏi huyền phù, do đó làm giảm nồng độ chất gây ô nhiễm trong đất còn lại. Nước bị ô nhiễm tạo ra từ rửa đất được xử lý bằng công nghệ hiệp với các chất gây ô nhiễm.
Ly trích axit là một công nghệ ex situ sử dụng một hóa chất chiết xuất như axit hydrochloric hoặc axit sunfuric để chiết xuất chất gây ô nhiễm từ một ma trận rắn bằng cách hòa tan chúng trong axit. Các chất gây ô nhiễm kim loại được thu hồi từ dung dịch lọc axit bằng các kỹ thuật như pha nước điện phân.
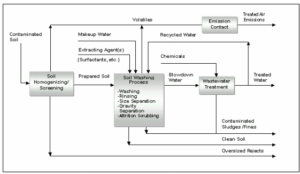
vận dụng:
- Đất ( ex situ )
- Trầm tích ( ex situ )
Các tác nhân được sử dụng trong rửa đất và chiết xuất axit:
- Chất tẩy rửa
- Chất hoạt động bề mặt
- Axit – Axit clohydric, axit sunfuric
- Tác nhân chelating
- Natri clorua
3. Xử lý nhiệt
biểu thị: Các quy trình xử lý nhiệt là phương pháp vật lý để loại bỏ thủy ngân khỏi môi trường bị ô nhiễm. Nhiệt được cung cấp dưới áp suất thấp cho đất hoặc chất thải bị ô nhiễm, thủy ngân bay hơi. Khí thải được xử lý bằng cách ngưng tụ để tạo ra thủy ngân nguyên tố lỏng.
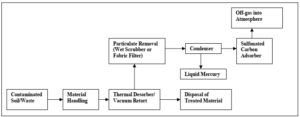
vận dụng:
- Đất
- Bùn
- Trầm tích
- Chất rắn khác
Các loại hệ thống xử lý nhiệt:
- Lò quay – đốt
- Vít nóng hoặc khoan – dầu nóng hoặc hơi nước
- Retort – sưởi điện dẫn điện hoặc đốt nhiên liệu
4. Thủy tinh hóa
trình diễn.#: Thủy tinh hóa là phương pháp xử lý nhiệt độ cao được thiết kế để cố định các chất gây ô nhiễm bằng cách kết hợp chúng trong sản phẩm cuối đông lạnh, có độ bền hóa học và chống rỉ nước. Phần cặn chính được tạo ra bởi công nghệ này thường là mảnh thủy tinh hoặc tổng hợp. Dư lượng thứ cấp được tạo ra là khí thải, chất gột rửa, lọc carbon… Quá trình này cũng có thể làm cho các chất gây ô nhiễm bay hơi hoặc trải qua sự phá hủy nhiệt, do đó làm giảm nồng độ của chúng trong đất hoặc chất thải.
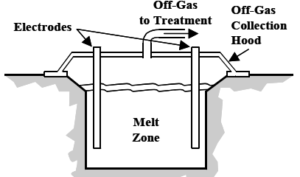
Áp dụng:
- Đất
- Trầm tích
Nguồn năng lượng được sử dụng cho thủy tinh hóa:
- Nhiên liệu hóa thạch
- Nhiệt trực tiếp
Cơ chế cung cấp năng lượng được dùng cho thủy tinh hóa:
- Hồ quang
- Đuốc plasma
- Lò vi sóng
- Điện cực (tại chỗ)
Độ sâu Áp dụng trong in situ:
- Độ sâu trình bày tối đa là 20 feet
- Độ sâu rất sâu hoặc độ sâu lớn hơn 20 feet có thể yêu cầu kỹ thuật cao
5. Kết tủa và đồng hóa
Mô tả:
Kết tùa sử dụng hóa chất để biến đổi các chất gây ô nhiễm hòa tan thành một chất rắn không hòa tan. Trong sự đồng hóa, chất gây ô nhiễm mục tiêu có thể ở dạng hòa tan, keo, hoặc hình thức treo. Các chất ô nhiễm hòa tan không kết tủa, nhưng được hấp phụ lên các chất khác dưới dạng kết tủa. Các chất ô nhiễm keo hoặc lơ lửng trở thành bị lẫn với các kết tủa khác loại hoặc được loại bỏ thông qua các quá trình như đông và keo tụ. Quy trình để loại bỏ thủy ngân từ nước có thể bao gồm kết hợp của kết tủa và sự đồng hóa. Chất rắn kết tủa /
đồng hóa sau đó được loại bỏ khỏi pha lỏng bằng cách lọc.
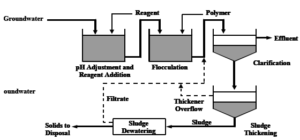
vận dụng:
- Nước ngầm
- Nước thải
Hóa chất và phương pháp được dùng để kết tủa / đồng hóa thủy ngân:
- Muối sắt (tỉ dụ, clorua sắt), sắt sunfat hoặc hydroxit sắt
- Phèn chua
- Điều chỉnh pH
- Vôi mềm, đá vôi và canxi hydroxit
- lưu hoàng
- Dẫn xuất Lignin
6. Hấp phụ
diễn tả: Trong hấp phụ, các chất hòa tan (chất gây ô nhiễm) tụ hợp ở bề mặt của một chất hấp phụ, do đó làm giảm nồng độ của chúng trong pha lỏng. Chất hấp phụ thường được đóng gói vào một cột. Các chất ô nhiễm được hấp phụ khi nước bị ô nhiễm được truyền qua cột.
Sự hấp phụ của các phân tử có thể được biểu diễn dưới dạng phản ứng vật lý:
A + B ↔ A•B
Trong đó:
A là chất bị hấp phụ (chất gây ô nhiễm)
B là chất hấp phụ
A•B là = Các hợp chất hấp phụ
vận dụng:
- Nước ngầm
- Nước uống
- Nước thải
Các loại chất hấp phụ được dùng để xử lý thủy ngân:
- Than hoạt tính dạng hạt
- Than hoạt tính ngâm tẩm diêm sinh
- Lọc Lancy
7. Lọc màng
diễn đạt: Lọc màng ngăn cách các chất ô nhiễm với nước bằng cách thông qua một hàng rào bán thấm hoặc màng. Màng cho phép một số thành phần đi qua trong khi chặn những thứ khác.
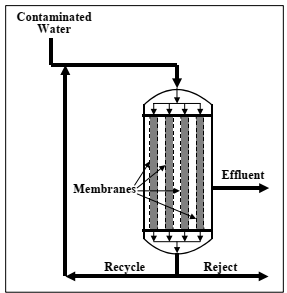
vận dụng:
- Nước uống
- Nước ngầm
- Nước mặt
- Nước thải công nghiệp
Các loại quy trình lọc màng:
- Vi lọc
- Siêu lọc
- Lọc nano
- Thẩm thấu ngược
8. Xử lý sinh vật học
biểu hiện: Xử lý sinh vật học các chất thải bị nhiễm thủy ngân được xúc tác bởi enzyme vi sinh vật. Trong một quá trình, chất tan, dạng ion của thủy ngân được sinh vật hiếu khí chuyển đổi thành thủy ngân nhân tố không hòa tan bởi một enzyme gọi là thủy ngân reductase. Các thủy ngân nhân tố ít hòa tan phải được chiết xuất bằng công nghệ khác. Trong một quá trình khác, sự phối hợp của phương pháp xử lý hiếu khí và kỵ khí được dùng để chuyển đổi các dạng thủy ngân hòa tan thành không hòa tan các pha khoáng, như sunfua. Nước thải từ hệ thống xử lý sinh học thường được xử lý thêm bằng than hoạt tính hoặc kết tủa trước khi xử lý.

ứng dụng:
- Nước thải
Vi khuẩn được sử dụng:
- Các chủng Pseudomonas spp chịu thủy ngân.
- Vi sinh vật nuối cấy độc quyền
Nguồn dinh dưỡng được sử dụng:
- Sucrose
- Chiết xuất nấm men
- NaCl
- Thuốc thử kiểm soát pH, như NaOH và H3PO4
- H2S
Các loại kỹ thuật được dùng:
- Lò phản ứng sinh vật học hiếu khí trên nền một mực (fixed-bed)
- Lò phản ứng sinh học cố định trên nền, với một loạt các bước xử lý hiếu khí và kỵ khí
Chất liệu đóng gói trong fixed-bed:
- Al2O3 và SiO2
- Môi trường gốm xốp
Nội dung trên đây là những phương pháp hay kỹ thuật cơ bản dùng để tiêu độc thủy ngân từ đất, nước và không khí. nhìn sẽ giúp ích cho các bạn phần nào trong mai sau. Ngoài ra còn có những phương pháp hiện đại khác, tuy nhiên tốn rất nhiều phí tổn và công nghệ để xử lý. Lần sau nếu có ai hỏi về chúng thì hãy nhớ về hóa học đằng sau nhé!
Tham khảo EPA và Zhongguo câu .